#accesibilidad Letra C centrada en la parte superior con cuatro puntos a su alrededor, dos horizontalmente y dos verticalmente. A continuación se muestra una representación de la estructura química de una molécula de hexano.
Cuando hablamos del ‘carbono’ pronto viene a la mente el grafito del lápiz, el gas carbónico que exhalamos por los pulmones, el diamante del anillo de brillante, la materia orgánica que compone animales y árboles, los nanotubos de carbono que… ¡¿NANOTUBOS DE CARBONO?!
El carbono es uno de los elementos químicos más versátiles de la Tabla periódica, presentándose en la naturaleza de varias formas, en estado sólido, líquido o gaseoso. Esto es fácilmente comprobado en el petróleo, de donde es posible extraer tanto el gas de cocina (GLP), moléculas ligeras con pocos átomos de carbono, como el asfalto, un sólido constituido de moléculas pesadas con muchos átomos de carbono. Debido a sus características químicas es capaz de formar también largas cadenas y gigantescas moléculas (arreglos supramoleculares) con miles de átomos de ese elemento. Por ejemplo, el plástico que está tan presente en nuestro día a día no es más que varias moléculas enormes estructuradas por enlaces químicos entre átomos de carbono. No obstante, el ADN es también una larga corriente constituida por pequeños eslabones (bases nitrogenadas) ligados por medio de átomos de carbono, resaltando que esas bases, a su vez, están constituidas también por átomos de otros elementos, como oxígeno y nitrógeno. Aunque formen enlaces con átomos de otra naturaleza, cuando forman estructuras compuestas sólo por carbonos (sustancias simples) se organizan en arreglos geométricos de varias formas. Sin lugar a dudas, el carbono es un elemento muy especial y su habilidad polimórfica gana un nombre exclusivo: los científicos la llaman de Alotropía.
Los átomos de carbono “tienen el derecho” de hacer cuatro conexiones con otros átomos, pudiendo ser de carbono o de otros elementos compatibles. En muchos casos hacen conexiones dobles, triples o incluso forman ciclos y anillos, dando origen a materiales con propiedades muy diferentes entre sí. Esta diversidad puede ser claramente observada al comparar el diamante, una gran estructura tridimensional formada por pequeños tetraedros, al grafito, formado por hojas planas estructuradas por hexágonos de átomos de carbonos conectados, expresando de esta forma su habilidad de Alotropía.
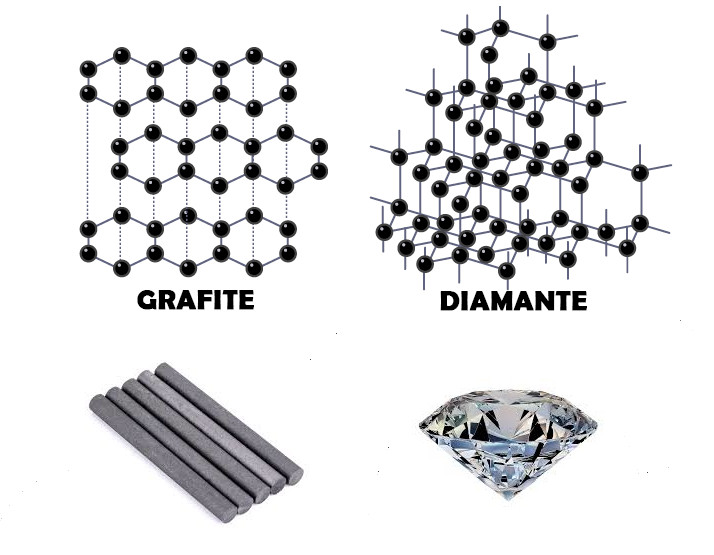
#accesibilidad De izquierda a derecha: en la parte superior, representaciones esquemáticas de las estructuras químicas del grafito y el diamante donde los átomos son bolas negras y los enlaces son líneas que conectan los átomos. En la parte inferior, palos de grafito y una gema de diamante.
En efecto, se descubrió recientemente una nueva forma alotrópica del carbono muy peculiar e interesante, los nanotubos de carbono (NTC). ¡Eso mismo! Son tubos muy, muy, muy pequeños, compuestos sólo por átomos de carbono. Lo más interesante de esta nueva estructura carbonácea son sus características, pues estos tubos logran conducir muy bien electricidad y calor. En comparación con los metales que también poseen estas propiedades, los NTC presentan grandes ventajas, por ejemplo, son más leves que los metales y la mayoría de las veces tienen mayor superficie de contacto. Además, el hecho de ser muy pequeños, tamaño de escala nanométrica (1 nanometro = 0,000000001 metro), hace de ellos muy prometedores para su utilización en nanotecnología. Algunos científicos ya están construyendo robots (dispositivos electrónicos) nanométricos constituidos por NTC. Investigadores en el área de la medicina ya están estudiando nanosondas biológicas compuestas por nanotubos de carbono para fines de identificación y tratamiento de enfermedades. Con ello, el descubrimiento y las aplicaciones de los nanotubos son una gran revolución en los materiales de carbono y también en la ciencia de los materiales.
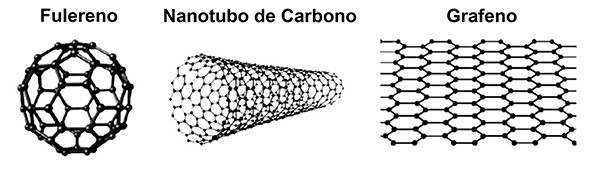
#accesibilidad De izquierda a derecha: representación de las estructuras de materiales fullerenos, nanotubos de carbono y grafeno.
Sin embargo, todavía hay muchos estudios que deben ser realizados y nuevos descubrimientos por delante, pues la cantidad de estudios acerca de ese material aumenta más cada año. Por último, vale resaltar que existen otras formas alotrópicas del carbono además de aquellas citadas aquí que también son muy interesantes y que poseen propiedades bien diferentes, por ejemplo, el grafeno y el fulereno. Toda la versatilidad de este elemento químico hace posible un gran número de aplicaciones de sus formas alotrópicas y, también, la consolidación de una gran área del conocimiento científico, la ciencia del Carbono.
Fuentes:
Fuente de la imagen destacada: Internet.
ATKINS, P. W., JONES, L., Princípios de Química: Questionando a Vida Moderna e o Meio Ambiente, 5ª edição, Editora Bookman, 2011.
Para saber más:
https://www.youtube.com/watch?v=tZJzKz5Z8kw
https://deepcarbon.net/dco/deep-carbon-science
https://www.youtube.com/watch?v=NoKE7uluZuc
Otros disseminadores:
https://pt-br.facebook.com/cienciausp/



Muito legal
Texto bastante explicativo e interessantíssimo! Muito bem escrito e completamente pertinente.